|
近年来癌症免疫领域持续升温,已然掀起癌症研究及治疗的一场“革命”。然而,癌症的免疫治疗仅对部分病人有效,如何快速高效的筛选到治疗有效的病人,为病人尽可能缩短寻找合适药物的时间,同时尽可能减少无效的治疗费用,逐渐成为免疫治疗领域的研究热点。 2015年Science发表的文章中,使用全外显子组测序(whole exome sequencing)及转录组测序(whole transcriptome sequencing)分析已转移黑色素瘤病人不同基因型对于Ipilimumab治疗效果的影响,找到一些可用于免疫治疗病人筛选的证据。让我们一起来学习一下这个重磅新发现吧! 背景: 虽然2011年FDA已经批准Ipilimumab单抗上市,用于治疗晚期黑色素瘤,但仅有20%的病人使用后能明显改善预后。 Ipilimumab单抗能有效阻滞一种叫做细胞毒性T细胞抗原-4(CTLA-4)的分子。CTLA-4可抑制T淋巴细胞活化。Ipilimumab通过与CTLA-4结合,阻碍CTLA-4与配体CD80/CD86相互作用,进而增加T细胞的活化和增殖。 研究目标: 寻找已转移黑色素瘤病人中可预测Ipilimumab单抗治疗效果和预后的临床基因表型。 材料与方法: 1、110例接受Ipilimumab治疗的已转移黑色素瘤的病人活检样本进行全外显子组测序(whole exome sequencing)。 2、其中40例病人进行转录组测序(whole transcriptome sequencing)。 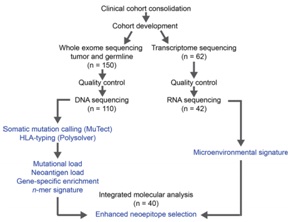
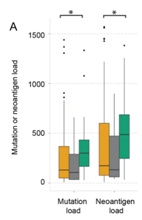 
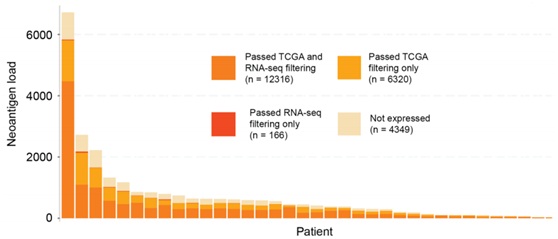
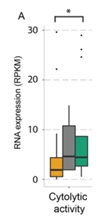 1、首次阐明了新生抗原(Neoantigen)的数量、细胞毒活性基因、免疫检查点基因的表达量有可能在癌症的免疫治疗中发挥重要作用。 2、更为重要的是,全外显子组测序(whole exome sequencing)和转录组测序(whole transcriptome sequencing)联合分析更有利于找到癌症免疫疗法应答/抵抗基因,为临床筛选免疫治疗敏感的病人提供理论依据。 参考文献: Genomic correlates of response to CTLA-4 blockade in metastatic melanoma. Science. 2015 Oct 9;350(6257):207-11. doi: 10.1126/science.aad0095. |








